Synthèse
L’adoption croissante des tests rapides effectués sur les lieux de soin (PoC — Point of Care) a considérablement accru le nombre de diagnostics in vitro (IVD — In Vitro Diagnostic) réalisés en dehors des environnements de laboratoire automatisés. Dans le présent article, nous explorons les défis de sûreté et de sécurité que soulèvent les tests exécutés sur les lieux de soin et les conséquences de la réutilisation des dispositifs de test ou de l’emploi illicite des échantillons, avant d’expliquer comment les fabricants peuvent minimiser les risques en optant pour des circuits intégrés d’authentification sécurisés.
Introduction
Pendant de nombreuses années, les tests de diagnostic effectués sur des échantillons humains étaient exclusivement traités dans des laboratoires cliniques. L’adoption des tests réalisés directement sur les lieux de soin change la donne en confiant la gestion des échantillons à un médecin, une clinique ou un hôpital, voire au patient en personne. Les tests PoC présentent plusieurs avantages : ils accélèrent le diagnostic en évitant d’envoyer les échantillons à un laboratoire et améliorent de façon significative les flux de travail tout en étant plus pratiques pour le patient. La nécessité de disposer de tests PoC robustes s’est imposée pendant la pandémie de COVID-19, lorsque les retards dans le traitement des tests ont eu un impact majeur sur la société, contribuant notamment à la propagation du virus au cours des premiers mois de la crise sanitaire.
Les tests effectués sur les lieux de soin ont un bel avenir devant eux et dans ce contexte, les fabricants de matériel de diagnostics élargissent leur portefeuille de tests en incluant des cibles multiples, telles que les panels respiratoires, les maladies sexuellement transmissibles (MST), les infections sanguines, etc. À mesure que ce marché se développe, le nombre d’échantillons de patients traités hors des laboratoires connaît une progression régulière. Or, ces échantillons sont à présent manipulés non seulement par des professionnels dans le cadre de flux de travail étroitement contrôlés, mais également par des médecins en environnement hospitalier, voire par les patients eux-mêmes à domicile, de sorte que le risque d’utilisation erronée et de réutilisation augmente de manière sensible.
Défis liés aux tests PoC : risques de réutilisation, de mauvaise utilisation et de contrefaçons
Pour tirer pleinement parti des avantages offerts par les tests effectués sur les lieux de soin, les systèmes disponibles doivent produire un résultat auquel les patients et les médecins peuvent se fier. À ce titre, la précision des mesures est un critère essentiel, dans la mesure où un résultat imprécis risque de provoquer des erreurs de diagnostic. Par ailleurs, un test même précis risque de générer un diagnostic erroné si l’échantillon ne correspond pas au patient traité. Pour obtenir un résultat fiable et réduire les risques d’erreur, il est par conséquent impératif de garantir l’intégrité des échantillons.
La possibilité de réutiliser des échantillons est un facteur de risque majeur : c’est le cas lorsqu’un écouvillon ou une cartouche est accidentellement traité plusieurs fois par le dispositif de test. Prenons l’exemple d’une cuisine où chaque membre de la famille effectue un test avant de prendre le chemin du bureau et de l’école. On imagine sans difficulté que l’un des parents peut « accidentellement » réutiliser un même écouvillon avec un autre enfant. Ce risque est également présent dans les cliniques ou dans les laboratoires non certifiés CLIA1 qui ne sont pas tenus de faire appel à des laborantins professionnels pour procéder aux tests de diagnostic.
L’utilisation malveillante d’un échantillon constitue un deuxième risque important. Concernant certains tests visant par exemple à identifier la présence de médicaments illégaux, les patients peuvent être tentés de falsifier les résultats. La substitution de la cartouche d’échantillon avant le traitement constitue l’un des moyens d’y parvenir. Par ailleurs, l’achat de cartouches contrefaites est un obstacle à l’obtention de résultats précis. Si les laboratoires traditionnels ont recours à des circuits d’achat qualifiés, les patients qui effectuent eux-mêmes les tests à domicile s’approvisionnent souvent sur Internet, ce qui ouvre la voie aux fournisseurs de contrefaçons dont les produits de qualité généralement inférieure génèrent des résultats à la fiabilité défaillante.
Toutefois, les laboratoires ne sont pas non plus à l’abri des erreurs. Après usage, les kits d’échantillonnage utilisés sont jetés en tant que déchets médicaux. Lorsque ces déchets sont collectés par un tiers, le risque existe que les kits d’échantillonnage soient reconditionnés avant d’être remis sur le marché. Mais s’ils semblent neufs, ces kits ne contiennent souvent pas d’agent réactif ou sont simplement remplis d’eau, contribuant ainsi à fausser le résultat des tests et, potentiellement, à prescrire au patient un traitement inadapté.
La réutilisation, de même que l’utilisation malveillante ou simplement erronée d’échantillons, peut avoir un impact sur les patients comme sur les fabricants de dispositifs. En effet, les patients sont potentiellement victimes d’un diagnostic faussé — par exemple, un test déclaré à tort positif entraînera un traitement inutile. À l’inverse, un faux négatif repoussera l’établissement du diagnostic et, à terme, provoquera le retard ou l’absence de traitement. De leur côté, les fabricants de dispositifs peuvent être fortement pénalisés, que ce soit sous la forme d’une atteinte à leur réputation, de l’identification erronée de leurs produits comme étant inexacts, voire, dans le pire des cas, du rappel de leurs produits. La prévalence des cartouches contrefaites constitue un problème commercial considérable pour les fabricants de dispositifs de test, avec notamment la possibilité de perturber le flux de recettes que constituent les cartouches jetables.
Atténuer les risques liés aux tests PoC : une impasse pour les solutions classiques
Deux méthodes permettent de garantir l’authenticité des échantillons de patients. Primo, l’étiquetage par codes-barres 1D ou 2D. Secundo, l’utilisation de caractéristiques mécaniques empêchant la réinstallation d’une cartouche. La première méthode est privilégiée pour le suivi des échantillons en laboratoire. Les informations relatives aux lots de fabrication, aux numéros de série et à l’identification unique des dispositifs peuvent être utilisées pour garantir l’authenticité de la cartouche. En outre, les codes-barres peuvent être examinés avant de traiter les échantillons dans l’optique de vérifier que le dispositif n’a pas été utilisé antérieurement. Mais s’ils constituent un moyen efficace de garantir l’authenticité de l’échantillon, les codes-barres présentent certaines contraintes : tout d’abord, un lecteur de codes-barres est indispensable, ce qui complique la conception de l’instrument en raison des exigences de dimensions et de distance focale. De plus, les codes-barres requièrent une importante mémoire pour stocker un nombre suffisant de numéros de série afin d’éviter toute réutilisation. Ce n’est pas un problème pour les machines de grandes dimensions utilisées en laboratoire, mais un défi de coût et de taille pour les équipements PoC compacts. Enfin, les codes-barres sont visibles par l’utilisateur, ce qui les rend moins sûrs et augmente les risques de copie ou de falsification.
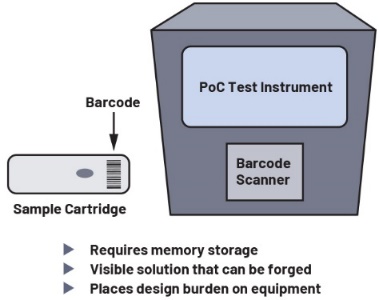
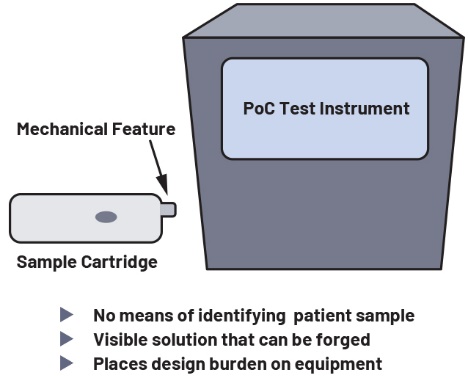
La seconde méthode consiste à utiliser une simple caractéristique mécanique, par exemple une encoche dans la cartouche qui change de forme ou de position après avoir été insérée dans l’instrument. Ces solutions mécaniques constituent un moyen simple d’empêcher la réutilisation et peuvent être mises en œuvre à faible coût. Toutefois, elles sont identiques d’une cartouche à l’autre, ce qui ne permet pas de faire la distinction entre différents échantillons, visibles par l’utilisateur, et généralement faciles à copier, rendant leur conception propice aux tentatives de contrefaçon. De plus, les caractéristiques mécaniques peuvent être réinitialisées lorsque des kits usagés sont reconditionnés par un intervenant malveillant. Enfin, les dispositifs de diagnostic sur les lieux de soin étant de plus en plus compacts, l’ajout d’une caractéristique mécanique ajoute une nouvelle contrainte de conception.
Qu’est-ce que l’authentification électronique ? Comment améliore-t-elle le résultat des tests PoC ?
Sur le marché des tests de diagnostic effectués sur les lieux de soin, la solution idéale se trouve ailleurs, à savoir sous la forme d’un circuit intégré à authentification électronique incorporé dans la cartouche. Un circuit intégré d’authentification électronique est un moyen efficace de prévenir l’utilisation répétée et/ou malveillante des cartouches. En ce qui concerne les risques de réutilisation, les circuits intégrés d’authentification électronique contiennent des compteurs décrémentiels sécurisés qui garantissent que les cartouches à usage unique sont effectivement utilisées une seule et unique fois. L’intégration d’un code numérique exclusif permet d’identifier l’échantillon d’un patient par rapport à un autre. Le risque d’utilisation malveillante est également pris en compte grâce à l’incorporation d’algorithmes de type « challenge-réponse » basés sur le chiffrement qui empêchent toute contrefaçon des cartouches. Les circuits intégrés d’authentification sécurisés disposent en outre de fonctions supplémentaires, telles que la possibilité d’enregistrer en toute sécurité l’historique d’utilisation sous forme horodatée — une fonction qui peut s’avérer précieuse lorsque les tests doivent être effectués quotidiennement à plusieurs reprises et à des horaires précis.
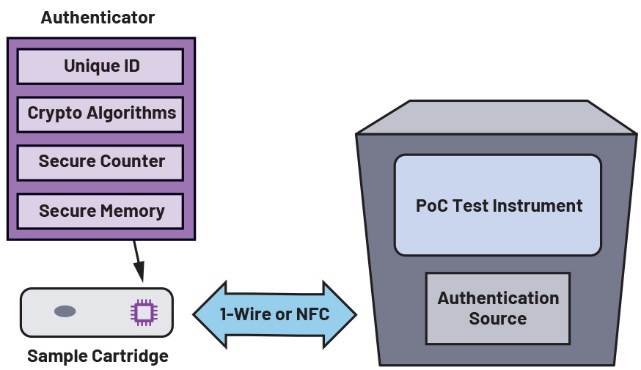
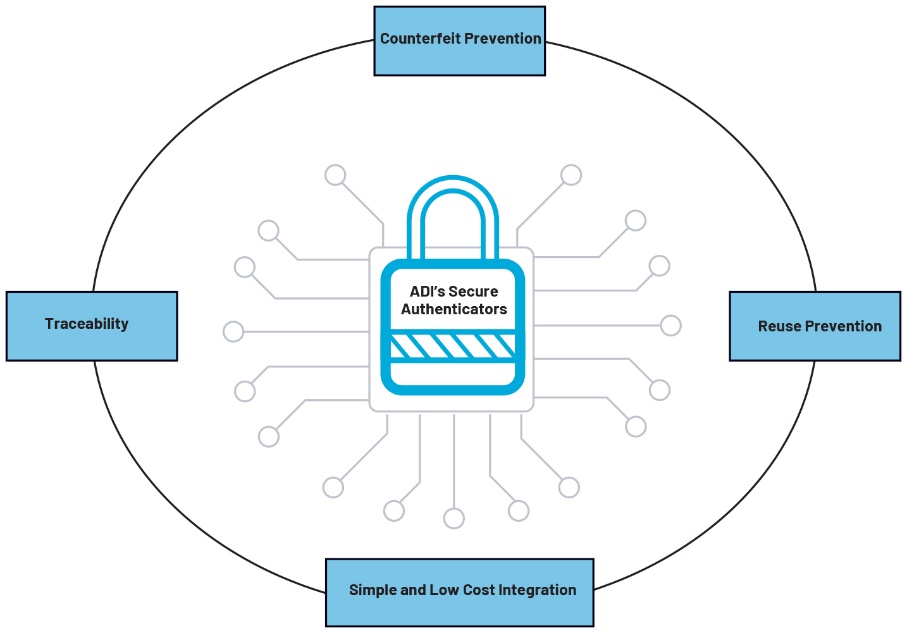
Contrairement aux codes-barres et aux caractéristiques mécaniques, les circuits d’authentification électronique sont intégrés à la cartouche, de sorte que la solution de sécurité est invisible pour les utilisateurs et d’éventuels contrefacteurs. De plus, un circuit intégré compact minimise les problèmes de conception liés aux contraintes de dimensions qui caractérisent les instruments de diagnostic de faibles dimensions utilisés sur les lieux de soin.
L’adoption d’un circuit intégré d’authentification électronique réduit de façon significative les risques de réutilisation et d’utilisation erronée ou malveillante des cartouches d’échantillons, garantissant aux patients et aux fabricants l’intégrité et la fiabilité du résultat des tests.
Solutions d’authentification électronique d’Analog Devices
Avec sa gamme de circuits intégrés d’authentification électronique, Analog Devices propose des solutions clé en main qui peuvent facilement être intégrées dans une cartouche PoC sans nécessiter de connaissances approfondies en chiffrement.
Chaque circuit intégré d’authentification sécurisé possède un numéro de série unique sur 64 bits qui sécurise l’identification et la traçabilité de la cartouche ou du dispositif. La mémoire sécurisée protège les données sensibles — informations de fabrication et paramètres d’étalonnage, par exemple — et empêche toute falsification. La méthode d’authentification utilise des algorithmes de chiffrement symétrique (algorithmes de hachage SHA-2/SHA-3) ou asymétrique (algorithmes de signature numérique basés sur les courbes elliptiques ECDSA). Conformes aux standards de l’industrie, ces algorithmes garantissent l’authenticité des cartouches et empêchent l’utilisation de contrefaçons tierces. Un compteur intégré exclusivement décrémentiel et sécurisé simplifie la gestion de l’utilisation et interdit toute réutilisation des cartouches jetables. Les produits clés pour l’application PoC sont le circuit sécurisé SHA-3 DS28E16 qui utilise une simple interface de communications 1-Wire®, et le circuit d’authentification MAX66250 avec interface sans contact NFC. Les circuits intégrés d’authentification électronique d’ADI peuvent être intégrés à un projet de conception sans recourir à un circuit imprimé dédié, facilitant ainsi la conception de systèmes compacts pour les tests de diagnostic sur les lieux de soin.
Conclusion
L’essor des tests sur les lieux de soin multiplie les exigences de sécurité et de traçabilité des échantillons de patients. Compte tenu de la miniaturisation des dispositifs et de l’augmentation des facteurs de risque inhérents à ce type de tests, les moyens traditionnellement mis en œuvre pour assurer le suivi des échantillons, tels que les codes-barres dont l’utilisation est très répandue dans les laboratoires, ne sont plus suffisants. A contrario, un circuit intégré d’authentification électronique tel que le DS28E16 d’ADI simplifie la conception des instruments PoC et aide les fabricants à minimiser les risques de sûreté et de sécurité tout en réduisant les erreurs de diagnostic potentielles, les retards de traitement, voire le rappel de produits.
Par Aileen Cleary, responsable Marketing, Kris Panaro, ingénieur d’applications terrain, et Chang Liu, ingénieur d’affaires, Analog Devices
À propos des auteurs
Aileen Cleary est responsable marketing de la business unit Medical Instrumentation and Life Sciences d’Analog Devices. Elle se concentre sur le développement des activités et de l’innovation au travers d’engagements centrés sur le client. Aileen affiche plus de 15 ans d’expérience dans l’industrie des semiconducteurs, un secteur où elle a occupé diverses fonctions techniques et commerciales pour les marchés de l’énergie et de la santé. Aileen Cleary est titulaire d’une maîtrise en ingénierie électronique et électrique de l’université d’Édimbourg (Écosse).
Kris Panaro a rejoint ADI en 2021. En tant qu’ingénieur d’applications de terrain (FAE) pour la région Amérique du Nord-Est, Kris possède une solide expérience de la conception de dispositifs médicaux, notamment dans le domaine des diagnostics moléculaires. Kris Panaro est titulaire d’une licence en génie électrique de l’Université d’État de New York (Buffalo).
Chang Liu est directrice commerciale en charge des produits d’authentification sécurisés chez Analog Devices, et notamment du développement du marché en Amérique du Nord. Chang a rejoint Maxim Integrated (aujourd’hui rattaché à Analog Devices) en 2001 et participé au développement de diverses lignes de produits. Chang Liu est titulaire d’une maîtrise en génie électrique de la Texas A&M University, College Station (Texas).
Article proposé par com-trail.fr
